Imaginez un matin où, après une sortie trail intense, vous vous levez sans cette raideur familière dans les genoux. Où le craquement sinistre qui suit un match de foot serré n'est plus l'annonce d'une douleur chronique. Depuis des siècles, la médecine se heurte à un mur biologique infranchissable : si votre os se casse, il se soude ; si votre peau se coupe, elle se cicatrise ; mais si votre cartilage s'abîme, le silence radio s'installe pour toujours. Cette impasse pourrait bientôt appartenir au passé grâce à une découverte majeure annoncée en novembre 2025 par Stanford Medicine. Des chercheurs y ont identifié un interrupteur moléculaire capable de faire repousser ce tissu que l'on croyait condamné à l'usure irréversible.

Pourquoi votre cartilage ne se répare jamais (et ce que ça coûte à votre corps)
Le contraste est frappant entre la résilience de notre squelette et la fragilité de nos articulations. Frappez un os avec un marteau, il se brise mais l'organisme déploie une armada de cellules pour le reconstruire, souvent plus fort qu'avant. Entaillez votre cartilage, et rien ne se passe. C'est le seul tissu du corps humain qui ne possède pas la capacité de se réparer spontanément. Cette particularité biologique a des conséquences dévastatrices pour une génération active qui repousse toujours plus loin les limites de la performance physique. La raideur matinale après une course, le genou qui gonfle après une séance de sport, ce sont les signaux d'alarme d'un tissu qui s'use sans espoir de retour en arrière.
L'explication réside dans une caractéristique anatomique fondamentale : le cartilage est un tissu avasculaire. Pour le dire simplement, il n'y a pas de routes d'approvisionnement. Contrairement à la peau ou aux organes, il est dépourvu de vaisseaux sanguins, ces autoroutes qui transportent les nutriments et, surtout, les cellules réparatrices sur les lieux du dégât. C’est comme une ville coupée du monde extérieur : si une maison s'effondre, il n'y a pas de pompiers ni de maçons pour venir la rebâtir. Les dommages s'accumulent ainsi en silence, année après année, jusqu'à ce que l'os finisse par frotter directement sur l'os. Ce processus, que l'on nomme l'arthrose, est loin d'être une simple fatalité de la vieillesse. Il s'agit d'un problème de santé publique majeur qui touche 1 adulte sur 5 aux États-Unis et coûte la somme astronomique de 65 milliards de dollars par an en soins directs, selon les chiffres avancés par Stanford. Jusqu'à très récemment, la médecine moderne ne savait ni le réparer, ni le régénérer, se contentant de remplacer l'articulation usée par une prothèse.
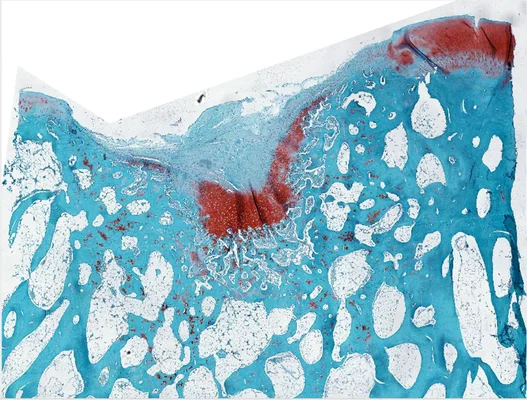
Un tissu sans ravitaillement : l'explication biologique d'une impasse médicale
Pour comprendre pourquoi cette découverte est si révolutionnaire, il faut saisir l'isolement anatomique du cartilage. Imaginez une éponge comprimée entre deux pierres. Cette éponge, c'est votre cartilage, et elle ne contient ni nerf, ni vaisseau sanguin. Elle vit en quasi-autarcie, nourrie lentement par le liquide synovial qui l'entoure. Lorsqu'une lésion survient, qu'il s'agisse d'un choc violent ou d'une usure progressive, le corps envoie le signal de l'alarme via l'inflammation. Cependant, les cellules souches, ces maçons capables de tout reconstruire, circulent dans le sang. Sans vaisseaux pour les acheminer jusqu'au cartilage abîmé, le chantier reste désespérément vide. C'est la raison pour laquelle, contrairement à la peau qui cicatrise toujours ou à l'os qui se ressoude, le cartilage reste muet face à l'agression. Cette nature avasculaire a longtemps été considérée comme une condamnation à perpétuité par la communauté scientifique, transformant toute lésion en dégât irréversible.
Arthrose et sport : quand le corps ne suit plus les ambitions
Cette réalité biologique heurte de plein fouet notre mode de vie actif. Les sportifs, qu'ils soient amateurs ou professionnels, soumettent leurs articulations à des contraintes répétées que le cartilage ne peut pas encaisser indéfiniment. Chaque saut, chaque changement de direction brusque, chaque impact crée des microtraumatismes. Chez un sujet jeune, le cartilage est épais et élastique, capable d'absorber ces chocs. Mais avec le temps et les répétitions, la structure se fragilise. Le drame, c'est que le dommage est cumulatif et invisible pendant des années. Un jeune footballeur qui se déchire le ligament croisé à 20 ans mettra le pied, sans le savoir, sur le chemin de l'arthrose. Jusqu'ici, la réponse médicale était décevante : des anti-inflammatoires pour masquer la douleur, des infiltrations de cortisones pour éteindre l'incendie temporairement, ou, à terme, la chirurgie prothétique. Nous palliions les symptômes sans jamais pouvoir s'attaquer à la cause racine : la disparition du tissu lui-même.
Novembre 2025 à Stanford : l'injection qui a fait repousser le cartilage
En novembre 2025, l'équipe de Stanford Medicine a publié les résultats d'une recherche qui pourrait bien réécrire l'histoire de la rhumatologie. Le récit commence là où personne ne cherchait vraiment : dans l'étude du vieillissement articulaire. Plutôt que de tenter de greffer des cellules étrangères ou d'implanter des matrices synthétiques complexes, les chercheurs ont décidé de regarder le cartilage non pas comme un matériau inerte, mais comme un tissu qui a oublié comment se renouveler. Ils ont découvert qu'en bloquant une seule protéine spécifique, le cartilage de souris âgées se mettait non seulement à se réparer, mais à croître à nouveau. C'est un peu comme si on avait trouvé le bouton « marche » d'une machine que l'on croyait en panne définitive.
La protéine en question se nomme la 15-PGDH (15-hydroxyprostaglandine déshydrogénase). Les scientifiques l'ont surnommée un « gérozyme », un terme fascinant qui désigne une enzyme dont l'activité spécifique est d'accélérer le vieillissement d'un tissu. La découverte de Stanford a été validée croisée par les NIH, les Instituts nationaux de la santé américains, ce qui lui confère une crédibilité scientifique considérable. L'impact de cette annonce réside dans sa simplicité apparente : là où des milliards avaient été investis dans des thérapies cellulaires complexes, Stanford a trouvé un simple interrupteur moléculaire accessible par une petite molécule. C'est un changement de paradigme total : au lieu de remplacer la pièce usée, on répare le moteur en place.
Le « gérozyme » 15-PGDH : l'enzyme que personne ne regardait
Pendant des années, la communauté scientifique s'était focalisée sur le manque de cellules souches dans le cartilage comme étant l'obstacle principal à la régénération. On cherchait désespérément des moyens d'apporter ces cellules de l'extérieur, par greffe ou par culture. Mais l'équipe de Stanford a eu une intuition différente : et si les cellules étaient déjà là, mais qu'on leur interdisait de travailler ? C'est là qu'intervient la 15-PGDH. Cette enzyme joue le rôle d'un frein biologique. Elle est présente tout au long de notre vie, mais son taux augmente drastiquement avec l'âge. En identifiant cette protéine comme le « coupable » de la paralysie régénérative du cartilage, les chercheurs ont changé la cible thérapeutique. Au lieu d'une ingénierie tissulaire lourde et coûteuse, on se tourne vers une approche pharmacologique, beaucoup plus simple à mettre en œuvre et potentiellement généralisable. Ce gérozyme agit comme un vieillard grincheux qui dirait aux cellules : « Reposez-vous, ne bougez plus, votre temps est passé ». L'injection découverte par Stanford a pour effet de faire taire ce vieux gardien.
Un résultat qui a surpris les chercheurs eux-mêmes
Au laboratoire, la surprise fut totale lorsque les premières images sont arrivées sur les écrans. Les chercheurs observaient des souris âgées, dont le cartilage avait naturellement diminué avec le temps. Après le traitement, les scans montraient un épaississement net et mesurable du cartilage dans les articulations. C'est un résultat qui, selon les canons de la biologie médicale, était jugé impossible jusqu'alors. On savait que certains animaux, comme le triton ou l'axolotl, pouvaient régénérer des membres, mais jamais on n'avait observé une telle régénération chez un mammifère adulte pour un tissu aussi avasculaire. Une chercheuse de l'équipe a résumé l'émotion du moment par une phrase qui résume tout l'espoir soulevé par cette étude : « Imaginez faire repousser le cartilage existant et éviter le remplacement articulaire ». Ce n'est pas juste une amélioration symptomatique, c'est une restauration structurelle. Le cartilage n'était pas juste « mieux protégé », il était revenu.
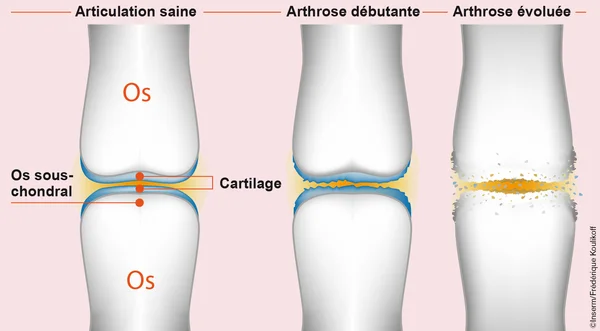
15-PGDH : comment cette protéine du vieillissement bloque la régénération (et comment la neutraliser)
Maintenant que l'émerveillement est passé, place à la compréhension du mécanisme. Comment une simple injection peut-elle inverser des années d'usure articulaire ? La clé réside dans une cascade biochimique en trois temps, que l'on peut expliquer sans jargon complexe. Premièrement, avec l'âge, le taux de 15-PGDH double dans notre organisme, et plus spécifiquement au niveau des articulations. Deuxièmement, cette enzyme a une mission précise : elle détruit une molécule essentielle appelée la prostaglandine E2 (PGE2). Imaginez la PGE2 comme le carburant de la jeunesse cellulaire, le signal qui dit aux cellules de se diviser et de reconstruire le tissu. En vieillissant, la 15-PGDH détruit ce carburant plus vite qu'il n'est produit, mettant le moteur à l'arrêt.
Troisièmement, et c'est là l'ingéniosité du traitement Stanford : en utilisant une petite molécule inhibitrice, on bloque l'action de la 15-PGDH. Résultat immédiat : les niveaux de PGE2 remontent en flèche. Face à cette abondance de carburant retrouvée, les chondrocytes (les cellules qui composent le cartilage) se réveillent. Ils se reprogramment en quelque sorte vers un état plus « juvénile », retrouvant une capacité de prolifération qu'ils avaient perdue depuis des années. Ce qui est absolument fascinant, c'est qu'il n'y a aucun recours à des cellules souches externes. Ce ne sont pas des cellules greffées qui font le travail, ce sont vos propres cellules, déjà présentes sur place, qui reprennent du service. C'est une démo de force de la biologie : on n'a pas eu besoin d'inventer une nouvelle cellule, juste de débloquer le potentiel latent de celle qui existait déjà.
Prostaglandine E2 : la molécule de la jeunesse que votre corps détruit avec l'âge
La prostaglandine E2, ou PGE2, est souvent connue du public pour son rôle dans l'inflammation et la douleur, d'où l'usage courant d'anti-inflammatoires qui bloquent sa production. Mais ici, nous découvrons l'autre face de cette molécule : celle de l'hormone de la reconstruction. Au sein de l'articulation, la PGE2 agit comme un messager chimique vibrant qui ordonne aux cellules cartilagineuses de se multiplier et de synthétiser la matrice extracellulaire, ce matériau glissant et amortisseur qui donne au cartilage ses propriétés uniques. Le problème n'est pas que le corps arrête de produire la PGE2 avec l'âge, mais plutôt que la 15-PGDH devient trop zélée. Elle dégrade la molécule avant qu'elle n'ait pu agir. C'est une dynamique classique du vieillissement : le potentiel est là, les ressources sont là, mais un mécanisme de freinage s'emballe. En inhibant ce frein, on restaure l'équilibre chimique de la jeunesse. C'est une découverte contre-intuitive : pour réparer, il faut rétablir une molécule que l'on associe souvent à l'inflammation. Cela montre à quel point la biologie est une affaire d'équilibre subtil plutôt que de simple suppression.
Sans cellules souches : pourquoi c'est une révolution conceptuelle
Se passer de cellules souches est un avantage pratique et théorique colossal. Jusqu'à présent, la plupart des pistes de recherche visant à régénérer des organes ou des tissus passaient par la greffe de cellules souches. Or, cette approche est semée d'embûches. Il faut prélever les cellules sur le patient (ou un donneur), les cultiver en laboratoire pendant des semaines, ce qui coûte cher et comporte des risques de contamination ou de mutation, puis les réinjecter. Sans parler du risque de rejet immunitaire. L'approche de Stanford contourne toutes ces difficultés. Puisque l'on réveille les cellules locales, le système immunitaire ne voit rien à redire : ce sont « ses » cellules qui travaillent. Il n'y a pas de rejet, pas de culture complexe, pas de prélèvement invasif. C'est une révolution conceptuelle car elle suggère que pour traiter la dégénérescence liée à l'âge, on n'a peut-être pas besoin d'apporter de la jeunesse de l'extérieur, mais simplement de libérer la jeunesse prisonnière à l'intérieur de nos propres tissus.
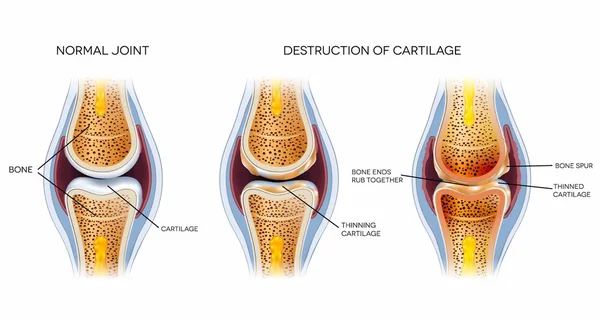
Deux injections par semaine pendant quatre semaines : le protocole qui a changé les genoux des souris
La théorie est séduisante, mais la médecine se prouve par la pratique. Le protocole expérimental mis en place à Stanford est remarquable par sa simplicité. Les chercheurs ont testé deux modes d'administration du traitement. Le premier, par injection intra-abdominale, a permis de traiter l'animal globalement. Le second, par injection intra-articulaire, consistait à piquer directement dans le genou de la souris. Les deux méthodes ont conduit au même résultat spectaculaire : un épaississement mesurable du cartilage. Cela laisse penser que dans le futur, on pourra peut-être choisir entre un traitement local pour une articulation précise (comme le genou d'un coureur) ou un traitement plus global pour les patients souffrant d'arthrose diffuse.
La posologie retenue lors de ces expériences était de deux injections par semaine pendant une durée de quatre semaines seulement. C'est une courte période pour un effet biologique aussi profond. Ce qui rend l'expérience particulièrement robuste, c'est le choix du modèle animal. Les chercheurs n'ont pas utilisé de souris juvéniles auxquelles ils auraient artificiellement endommagé le cartilage. Ils ont utilisé des souris âgées présentant une perte de cartilage naturelle, liée au vieillissement. C'est un détail méthodologique crucial. Chez une jeune souris, la régénération est souvent plus facile ; observer un tel effet chez des sujets âgés dont le tissu est usé par le temps suggère que le mécanisme pourrait fonctionner chez des humains adultes, voire âgés, et pas seulement chez de jeunes athlètes victimes d'un accident. C'est la preuve que l'horloge biologique peut effectivement être remontée en arrière.
Injection dans le genou ou dans le ventre : les deux voies testées avec succès
Le fait que l'injection directe dans le genou et l'injection dans l'abdomen fonctionnent toutes deux ouvre des perspectives thérapeutiques intéressantes. L'injection intra-articulaire est la plus logique pour un rhumatologue traitant un genou douloureux : elle permet de concentrer le produit exactement là où c'est nécessaire, probablement avec une dose plus faible et moins d'effets secondaires potentiels sur le reste du corps. Cependant, l'injection systémique (dans le ventre, qui diffuse ensuite dans le sang) offre un avantage majeur pour les patients polyarthrosiques, ceux qui souffrent des doigts, des genoux et des hanches en même temps. Une simple piqûre pourrait potentiellement traiter l'ensemble de l'organisme. Les chercheurs devront peser le pour et le contre lors des futurs essais humains : privilégier la précision ou la facilité d'usage. Mais avoir ces deux options sur la table dès le départ est un luxe en recherche médicale.
Souris âgées, pas souris de laboratoire juvéniles : pourquoi ce détail compte
Dans la recherche biomédicale, il est tentant de choisir les modèles les plus faciles. Créer une lésion chez un animal jeune et vigoureux est beaucoup plus simple que d'attendre qu'il vieillisse. Mais cette facilité a un prix : les résultats ne sont souvent pas transposables à l'humain moyen qui consulte son médecin à 50 ou 60 ans pour de l'arthrose. En utilisant des souris âgées, l'équipe de Stanford s'est assurée que le mécanisme de régénération n'était pas une caractéristique enfouie accessible seulement aux très jeunes organismes. Si le traitement avait marché sur des souris jeunes mais échoué sur des souris âgées, l'espoir pour les patients atteints d'arthrose liée à l'âge aurait été mince. Or, le fait que le cartilage usé par le temps puisse repousser signifie que le potentiel biologique ne s'évapore pas totalement, il est juste mis en sourdine. C'est une excellente nouvelle pour nous : cela signifie que nos articulations vieillissantes gardent en mémoire le plan de construction de leur jeunesse, attendant juste le signal approprié pour se remettre au travail.
Tissus humains de prothèses de genou : la preuve que le mécanisme fonctionne chez nous
Il est facile de rester sceptique face à des résultats obtenus chez la souris. Après tout, l'histoire de la médecine est remplie de traitements miraculeux chez le rongeur qui ont échoué chez l'homme. C'est pourquoi l'équipe de Stanford a poussé la démonstration un cran plus loin. Ils ne se sont pas contentés des modèles animaux. Des échantillons de cartilage humain ont été prélevés directement sur des patients subissant une opération de pose de prothèse de genou. Ces tissus, considérés comme « finis » par la chirurgie, ont été mis en culture en laboratoire et exposés au traitement inhibiteur de la 15-PGDH. Le résultat a été sans appel : les cellules humaines ont réagi exactement comme celles des souris, produisant du nouveau cartilage fonctionnel.
Cette étape est le pont critique entre la théorie et la réalité clinique. Elle prouve que le mécanisme biologique découvert chez l'animal est conservé chez l'humain. Mais il y a un autre élément rassurant : la sécurité. Des essais cliniques de Phase 1 avaient déjà été menés sur des humains pour tester un inhibiteur de 15-PGDH, mais pour une autre indication : la faiblesse musculaire liée à l'âge. Ces essais, visant à vérifier que le produit n'était pas toxique, ont été couronnés de succès, sans effets secondaires graves notables chez des volontaires sains. Cela signifie que le « médicament » en soi n'est pas une inconnue dangereuse. Nous savons déjà que bloquer cette enzyme est tolérable par l'organisme humain, ce qui pourrait considérablement accélérer le passage aux essais spécifiques pour le cartilage.
Du bloc opératoire au laboratoire : des tissus humains qui se remettent à fabriquer du cartilage
Le protocole utilisé sur les tissus humains est d'une élégance redoutable. Les chercheurs ont récupéré du cartilage issu de remplacements de genou, c'est-à-dire du tissu qui avait échoué à protéger l'articulation. Une fois au laboratoire, ce cartilage a été traité avec l'inhibiteur. Au microscope, ils ont observé la néo-synthèse : les cellules commençaient à sécréter à nouveau les molécules qui donnent au cartilage sa résistance et son élasticité. Ce n'est pas juste une multiplication cellulaire anarchique, c'est une reconstruction organisée. C'est la preuve de concept la plus directe que l'on puisse avoir à ce stade préliminaire. Elle dit : « Oui, vos cellules de cartilage, même celles qui sont usées par une vie d'activité, répondent encore au signal de la jeunesse ». Cela valide l'hypothèse que l'arthrose humaine n'est pas une mort cellulaire irréversible, mais une forme de « mise en veille » réversible.
Un inhibiteur de 15-PGDH déjà testé sans danger chez l'humain
C'est un atout stratégique majeur pour cette découverte. Habituellement, le développement d'un nouveau médicament prend une décennie, dont les premières années sont consacrées à tester la toxicité sur des animaux, puis sur de petits groupes d'humains pour voir si ça rend malade. Ici, comme un inhibiteur de 15-PGDH existe déjà (sous une forme orale) et a passé les premiers tests de sécurité pour des problèmes musculaires, le chemin est déjà partiellement dégagé. Bien sûr, il faudra refaire des essais spécifiques pour l'indication articulaire, car l'injection dans le genou ou la prise à long terme pour l'arthrose n'est pas la même chose qu'un traitement oral court pour le muscle. Mais le fait de savoir que l'on ne touche pas à une enzyme dont le blocage provoquerait des effets secondaires catastrophiques est un immense soulagement. Cela permet d'envisager les essais de Phase 2 (qui testent l'efficacité) avec une sérénité relative.
Déchirure du ligament croisé : comment cette découverte pourrait changer le destin des sportifs blessés
C'est sans doute la section qui parle le plus à notre public de jeunes actifs et de sportifs. La déchirure du ligament croisé antérieur (LCA) est une blessure cruelle, mais son véritable prix se paie souvent des années plus tard. Le chiffre est effrayant : selon certaines estimations, jusqu'à 87 % des patients ayant subi une déchirure du LCA développent de l'arthrose dans les 15 ans qui suivent l'accident. Pourquoi ? Parce que le traumatisme initial a endommagé le cartilage, et ce dernier, incapable de se réparer, continue de se dégrader silencieusement pendant des années, tandis que le ligament, lui, a été reconstruit chirurgicalement avec succès. Le sportif reprend sa compétition, le genou tient, mais l'horloge de l'arthrose tourne déjà.
L'équipe de Stanford a testé son traitement précisément sur ce scénario. Ils ont créé une lésion mimant une déchirure du LCA chez des souris et leur ont administré le traitement. Le résultat a été une réduction drastique du risque de développer une arthrose post-traumatique. Si ce résultat se transpose à l'humain, cela pourrait changer la prise en charge des blessures sportives. On imagine aisément un futur où, suite à une opération du genou pour une rupture du ligament, le patient ne suit pas seulement une rééducation kinésithérapique, mais reçoit aussi une série d'injections pour protéger et régénérer son cartilage. On passerait ainsi d'une médecine de réparation (du ligament) à une médecine de prévention de l'usure future (du cartilage). Cela pourrait sauver des milliers de carrières sportives et surtout éviter des décennies de douleur chronique.
87 % d'arthrosiques à 15 ans : le prix caché d'une déchirure du LCA
Il est crucial de bien comprendre la dynamique temporelle de cette blessure. Dans les semaines qui suivent l'accident, tout le monde se focalise sur le ligament. « Opéré ou pas ? », « Quand reprends-tu le sport ? ». Le cartilage est le grand oublié de ce drame. Pourtant, lors du choc, les surfaces articulaires se sont percutées avec violence, causant des microfissures et des contusions osseuses (œdèmes osseux) qui perturbent l'environnement du cartilage. Comme celui-ci ne se répare pas, ces lésions initiales vont s'étendre. La mécanique du genou, même une fois le ligament reconstruit, reste souvent légèrement altérée, ce qui crée des zones de surcharge. Le cartilage s'use là où il est trop sollicité. C'est pourquoi, 15 ans plus tard, un joueur de foot de 35 ans qui a eu son accident à 20 ans se retrouve avec un genou d'un vieillard de 70 ans. Traiter le cartilage dès la phase aiguë de la blessure pourrait briser ce cycle infernal.
Le protocole anti-arthrose post-traumatique testé à Stanford
L'expérience menée sur le modèle de lésion du LCA chez la souris a montré quelque chose de fascinant : le traitement ne se contentait pas de faire repousser du cartilage n'importe où. Il semblait cibler les zones lésées. En bloquant la 15-PGDH, les chercheurs ont permis aux cellules du cartilage adjacent à la lésion de proliférer pour combler la brèche. Dans les tests de suivi, les souris traitées montraient une épaisseur de cartilage beaucoup plus proche de la normale et beaucoup moins de signes d'inflammation chronique que les souris non traitées. Si un tel protocole était disponible pour l'humain, il pourrait être intégré dans la suite logique de la chirurgie ligamentaire : on répare le ligament, on soigne le cartilage. Cela transformerait l'orthopédie sportive en offrant une protection contre l'usure future, changeant ainsi radicalement le pronostic vital de ces athlètes pour leurs articulations.
Arthrose liée à l'âge : pourquoi cette injection ne signe pas (encore) la fin de la maladie
Face à une telle découverte, l'enthousiasme est naturel, mais la prudence scientifique reste de mise. L'arthrose n'est pas une maladie simple comme une infection bactérienne que l'on éradique avec un antibiotique. C'est une pathologie complexe, « multi-tissulaire ». Certes, le cartilage est l'acteur principal de la pièce, mais il ne joue pas seul. L'arthrose implique l'inflammation de la membrane synoviale (la membrane qui tapisse l'articulation), le remaniement de l'os situé juste sous le cartilage (l'os sous-chondral qui se densifie anormalement), et l'atrophie des muscles qui soutiennent l'articulation. Régénérer le cartilage est une pièce maîtresse du puzzle, peut-être la plus importante, mais ce n'est pas la seule.
En faisant repousser du cartilage, on résout certes le problème du frottement os contre os, mais quid de l'inflammation chronique qui ronge l'articulation ? Si l'os sous-chondral reste déformé et très dur, le nouveau cartilage sera peut-être plus épais, mais sera-t-il fonctionnel sur le long terme ? De plus, l'étude actuelle manque de recul. Nous savons que le cartilage repousse en quatre semaines chez la souris, mais nous ne savons pas ce qu'il advient de ce nouveau cartilage six mois ou un an plus tard. Est-il aussi résistant que le cartilage originel ? Il y a aussi la question des stades avancés de la maladie : quand l'arthrose est très avancée, l'articulation est déformée et instable. Remettre du cartilage dans une articulation bancale ne suffira peut-être pas à rendre une mobilité normale. Pour ces cas extrêmes, la prothèse restera probablement la solution pour longtemps encore.
Au-delà du cartilage : les autres acteurs de l'arthrose que l'injection ne traite pas
Il est essentiel de ne pas réduire l'arthrose à une simple « usure de la semelle » du genou. C'est une maladie de l'articulation entière. La membrane synoviale, par exemple, devient inflammatoire et produit des enzymes qui digèrent le cartilage. Si l'on régénère le cartilage avec le traitement Stanford mais que l'on ne calme pas cette synovite, celle-ci pourrait très bien détruire le nouveau cartilage tout aussi vite qu'elle a détruit l'ancien. De même, l'os sous-chondral, l'os sur lequel repose le cartilage, subit des transformations micro-architecturales. Il devient plus dense, plus rigide, perdant sa capacité d'amortissement. Un cartilage neuf posé sur un os trop dur, comme un tapis de luxe sur du béton, pourrait s'user prématurément. Enfin, les muscles autour du genou jouent un rôle d'amortisseur dynamique. S'ils sont faibles (ce qui est souvent le cas chez l'arthrosique sédentaire), la nouvelle surface articulaire subira de nouveau des contraintes excessives. Le traitement Stanford est une avancée immense, mais il devra probablement être couplé à une prise en charge globale (kinésithérapie, lutte contre l'inflammation) pour être vraiment optimal.
Les questions sans réponse : stades avancés, effets à long terme, doses répétées
La science avance par hypothèses et vérifications, et aujourd'hui, plusieurs zones d'ombre subsistent. Que se passe-t-il si le cartilage a totalement disparu, ne laissant que l'os nu à vif ? Les cellules cibles de la thérapie, les chondrocytes, ne sont plus là. Sans cellules à réveiller, le médicament peut-il encore agir ? C'est une question critique pour les stades les plus sévères de la maladie. Ensuite, la question de la durée : combien de temps l'effet dure-t-il ? Faudra-t-il faire une injection tous les ans, tous les cinq ans, ou une seule fois suffit-elle ? Et y a-t-il un risque que, en stimulant trop la croissance, on provoque une production excessive de cartilage, qui pourrait gêner la mobilité ou devenir une excroissance ? Ces questions ne sont pas des freins à l'espoir, mais des étapes obligatoires que les futurs essais cliniques devront franchir. La médecine est une affaire de balancier : trouver la dose qui guérit sans nuire.
Essais cliniques, commercialisation, prix : à quelle échéance pour une injection dans votre genou ?
C'est la question qui brûle les lèvres de tous les lecteurs : quand pourrai-je en bénéficier ? Il faut gérer son impatience. Les essais de Phase 1, qui testent la sécurité, sont déjà faits pour une version orale du produit. Mais pour une indication de régénération du cartilage, probablement par injection intra-articulaire, il faudra repasser par des phases d'essai spécifiques. Un essai clinique de Phase 2 (pour vérifier l'efficacité sur un petit groupe de patients humains) pourrait commencer dans les années à venir. Si les résultats sont positifs, la Phase 3 (essais à grande échelle) prendrait encore plusieurs années. En étant optimiste et en supposant que tout se passe parfaitement sans obstacle, on pourrait envisager une disponibilité sur le marché d'ici une demi-douzaine d'années. C'est long, mais court à l'échelle de l'histoire de l'arthrose.
Concernant le prix, il est impossible de donner un chiffre précis aujourd'hui, mais on peut se baser sur les biomédicaments injectables actuels (comme les anti-VEGF pour les yeux ou les anticorps monoclonaux pour les rhumatismes inflammatoires). Ces traitements coûtent souvent plusieurs milliers d'euros par cure. Cependant, la molécule ciblée par Stanford est une petite molécule chimique, potentiellement moins coûteuse à produire que des anticorps biologiques complexes. Le prix dépendra aussi beaucoup du mode d'administration et de la fréquence des cures. Pour l'accès en France, tout dépendra de son inscription sur la liste des produits remboursables par l'Assurance Maladie et de l'évaluation de son « service médical rendu ». Si le traitement permet réellement d'éviter des milliers de pose de prothèses chaque année, il serait économiquement rationnel pour le système de santé de le financer largement.
De la Phase 1 validée au protocole cartilagineux : le chemin clinique restant
Il ne suffit pas de dire « ça marche sur la souris et sur une cellule humaine en boîte » pour obtenir l'autorisation de vendre le médicament. Les autorités de santé, comme la FDA aux États-Unis ou l'EMA en Europe, exigent des preuves rigoureuses. Le médicament a déjà montré son innocuité par voie orale pour le muscle, mais l'injection dans le genou est une tout autre histoire. Il faudra prouver que le produit ne détruit pas l'articulation, ne provoque pas de tumeur ou d'infection grave. Ensuite, il faudra montrer qu'il est plus efficace que le placebo. Pour ce faire, les chercheurs devront probablement utiliser l'IRM pour mesurer l'épaisseur du cartilage des patients avant et après traitement, ce qui est techniquement difficile mais réalisable. Ce chemin est long, fastidieux et coûteux, mais il est nécessaire pour garantir que la solution miracle ne devienne pas un désastre sanitaire.
Prix et accessibilité : ce que l'on peut anticiper (et ce qu'on ne sait pas encore)
Le coût final de cette thérapie sera un facteur déterminant de son impact social. Si le prix est exorbitant, seuls une minorité pourront éviter la prothèse, creusant les inégalités face à la douleur. Les indications thérapeutiques joueront aussi un rôle : sera-t-il réservé aux arthroses débutantes, où le cartilage est encore présent (pour le « booster »), ou pourra-t-il être utilisé en urgence post-traumatique chez le jeune sportif ? Les scénarios sont multiples, et chacun aura un modèle économique différent. On peut espérer que, face à l'énorme coût économique de l'arthrose pour la société (perte de productivité, hospitalisations, prothèses), les acteurs de la santé favoriseront un accès large. Mais pour l'instant, tout cela reste spéculatif. Seuls les résultats des futurs essais permettront de définir la valeur réelle de ce traitement.
Ce qui change dès aujourd'hui, même sans l'injection
En attendant que les flacons arrivent dans les pharmacies, cette découverte transforme déjà notre rapport à la santé articulaire. Premièrement, elle brise le dogme fataliste : le cartilage peut repousser. Ce n'est plus une vue de l'esprit, c'est une preuve biologique publiée dans une grande revue. Deuxièmement, cela donne un sens immédiat à la préservation. Si des thérapies de régénération arrivent d'ici dix ans, alors protéger votre capital cartilagineux aujourd'hui a encore plus de valeur. On ne se bat plus pour reculer l'inévitable, mais pour préserver un terrain qui pourra être régénéré demain. Troisièmement, les jeunes sportifs blessés ont intérêt à suivre de près les essais cliniques à venir. La gestion d'une blessure grave pourrait changer radicalement dans un proche avenir. Finir sur une note d'espoir mesuré, sans promesse irréaliste, en rappelant que novembre 2025 à Stanford pourrait bien être la date que les rhumatologues retiendront comme le tournant.
Conclusion
L'annonce de Stanford Medicine en 2025 marque un tournant décisif dans notre compréhension et notre capacité à traiter la dégénérescence articulaire. En identifiant la protéine 15-PGDH comme le frein principal à la régénération du cartilage, et en prouvant que son blocage permet aux tissus de retrouver une jeunesse perdue, les chercheurs ont ouvert une voie thérapeutique jusqu'ici inimaginable. Cette découverte est d'autant plus prometteuse qu'elle s'appuie sur un mécanisme naturel, sans recours complexe aux cellules souches, et qu'elle a déjà montré son efficacité sur des tissus humains et un profil de sécurité acceptable lors d'essais précédents.
Cependant, le chemin vers une disponibilité thérapeutique large est encore long. Entre les essais cliniques de Phase 2 et 3 nécessaires pour valider l'efficacité et la sécurité spécifiques sur l'articulation humaine, et les questions inhérentes à la prise en charge d'une maladie complexe comme l'arthrose, plusieurs années s'écouleront avant que l'injection ne devienne une pratique courante. Il est également crucial de rappeler que cette injection, si elle parvient sur le marché, sera probablement un outil puissant parmi d'autres, nécessitant toujours une prise en charge globale incluant l'activité physique et la prévention. Néanmoins, l'espoir soulevé par ces travaux est rationnel et tangible. Le cartilage n'est plus une condamnation à vie, et cela change tout pour des millions de patients à travers le monde.